Micella
| Quell articol qì l'è scrivud in Lombard, cond l'ortografia Scriver Lombard. |
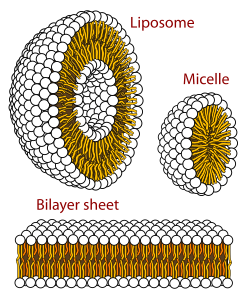
Una micella l'è un agregad (o assemblad soramolecolar) de molecole de tensioativ disperdide ind un colloid liqued. La micella tipega l'è un agregad qe el se forma ind una soluzion aquosa indov qe i coo idrofil i è in contait cond el solvent (l'aiva), e le coe le se strenj intra de lore in el center de la micella, qe se ge dix core. Qell comportament qé l'è doxid al fait qe i tensioativ con una cadena idrofoba i g'ha la tendenza a "impaqetar-s" intra de lor a formar agregads soramolecolar; come qe i fa fadiga a impienesser tœt el volœm del strat dope, e come qe i coo idrofii de solet i è plœ grands de le coe idrofobe, i se met insema a formar una micella, ma segond la forma del tensioativ i pœl formar anca oltre struture sora-molecolare. La micella qé descrivida l'è la micella plussee comuna (micella oi-in-aiva); le micelle roverse le g'ha inveci el grœp del coo al center, e le coe qe le varda de fœra invers la fas oleosa (micelle aiva-in-oi). Le micelle le se pœl considerar sferege. La forma e la dimension de una micella i è funzion de la geometria molecolara de le molecole de tensioativ qe i le fa sœ, e anca de le condizion de la soluzion, 'me prexempe el pH, la temperadura e la forza ionega. El process de formazion de le micelle l'è cognossid anca 'me micellizazion.
Storia
[Modifega | modifica 'l sorgent]La capacità de le soluzion de savon de comportar-s 'me deterjents la se cognoss de secoi. De tœte le manere, l'è domà al prencepe del secol XX qe i g'ha vambiad a studiar-ga adree a la composizion de qelle soluzion qé. El prim qe el g'ha studiad adree l'è stait el James William McBain a l'Università de Bristol; ind el 1913 el g'ha postulad l'esistenza de "ion colloidal" per spiegar la bona condutività eletrega de soluzion de palmitad de sodio. Qei insema de lavor qé, qe i se forma spontaneament e i è mobii fess, i è staits ciamads "micelle", un termen ciapad a prestet de la biolojia.
Solvatazion
[Modifega | modifica 'l sorgent]Ai singoi tensioativ qe i è ind el sistema ma i forma miga part de la micella se ge dix "monomer"; le micelle le representa un assemblad molecolar, indov qe ogne component individual de la micella istessa l'è ind un equiliber termodinameg cond i monomer de l'istessa specie ind el medium intoren. Ind l'aiva, i "coo" idrofil de le molecole de tensioativ i è semper ind contat cond el solvent, de manera miga dipendenta de se el tensioativ l'è in forma de monomer o l'è part de la micella; qell qe el cambia l'è el comportament de le coe idrofobe. Le coe idrofobe de faits le g'ha el minor contat cond l'aiva quand qe le tœl part a la micella, e qesta qé l'è donca la bas de la enerjia qe la porta a la formazion de una micella. Ind una micella, le coe idrofobe de tante molecole de tensioativ le se tœl ça insema a formar un core qe el somea una goça de oi, come qe l'è formad domà de le coe lipofii, qe i è plussee stabile perqè i è miga a contat cond la fas aquosa. Al istess temp, i monomer de tensioativ i è circondads de molecole de aiva ligade intra de lore de ligam a idrojen, qe le crea come 'na "gabia", ciamada "gabia de solvatazion". Qella gabia qé la g'ha una strutura qe la se insomea a qella dei cristai de giaz, e l'è a la bas del efet idrofobeg. Le micelle faite sœ de tensioativ ioneg le g'ha una atrazion eletrostatega invers ai ion arent a la micella ind la soluzion, qe se ge dix contraion. Istess qe i contraion plussee arent i pœl masqerar parzialment la carga de la micella (fina al 90%), i efets de la carca de la micella i modifega la strutura del solvent intoren fina a distanze importante de la micella. Le micelle ionege le inflœenza tante proprietà dela soluzion, intra le quai anca la condutività eletrega. A jontar-ga sai a un colloid qe el g'ha denter le micelle, se pœl sbassar la forza de le interazion idrostatege, e portar a la formazion de micelle ionege plœ grande.
Energia de formazion
[Modifega | modifica 'l sorgent]| Per savenn pussee, varda l'articol Termodinamega de la micellizazion. |
Le micelle le se forma domà quand qe la concentrazion de tensioativ la passa fœra la concentrazion micellara critega (CMC), e la temperadura del sistema l'è plœ granda de la temperadura micellara critega. Se riva a capir plœ ben la formazion de le micelle se se varda la termodinamega: le micelle le pœl formar-s deperlore perqè g'è un balançament intra l'entropia e l'entalpia. Ind l'aiva, l'efet idrofobeg l'è la forza guida per la formazion de le micelle, istess qe qell lavor qé l'è desfavoird de un pont de vista sies entalpeg qe entropeg ind el sistema.
Usaj
[Modifega | modifica 'l sorgent]Quand qe i tensioativ i è presents sota la concentrazion micellara critega (CMC) lor-qé i pœl far de emulsionants, qe i permet a un compost qe de solit l'è miga solubil (ind el solvent qe 'n s'è adree a doprar) de dissolver-s. Quell lavor qé el sœced perqè le specie insolubii le pœl vesser incorporade ind el core de la micella, qe l'è lu medem solubilizad ind el solvent grazia a le interazion dei coo dei tensioativ ind l'aiva. L'exempe plœ comun de qell fenomen qé i è i deterjents, qe i sneta materiai lipofii poc solubii ('me i oi e le cere) qe i pœl miga tirar-s via cond l'aiva apena. I deterjents i sneta anca perqè i sbassa la tension superfiçala de l'aiva, incé qe el sapes plœ facil el tirar vià un material da una superfis. La formazion de le micelle l'è essenziala anca per l'absorbiment de le vitamine lipofile e dei lipids compless denter al corp. I sai biliar qe i se fa sœ ind el fideg e i ven secreds de la cistifellea i permet la formazion de le micelle de acids grass. Qest lavor qé el permet l'absorzion de lipids complicads (prexempe lecitine) e vitamine liposolubii (A, D, E, K) denter le micelle ind el intestin pecen. Le micelle po, le se pœl doprar per el trasport de droge, 'me le nanopartexelle de or.
